近期,聂尧教授团队在利用非经典氨基酸理性提高酶蛋白的热稳定性方面取得重要进展,研究成果“Computational design of noncanonical amino acid-based thioether staples at N/C-terminal domains of multi-modular pullulanase for thermostabilization in enzyme catalysis”正式发表于Computational and Structural Biotechnology Journal (IF=7.271) (https://doi.org/10.1016/j.csbj.2020.12.043)。
酶的热稳定性是酶蛋白的一个重要特性,其可用于评估酶蛋白在工业应用的可行性,故酶蛋白的热稳定化被认为是生物合成中一个关键且通常必须的步骤。酶蛋白热稳定化的常规策略通常是引入由天然氨基酸取代引起的非共价相互作用和/或天然共价键来稳定酶蛋白。然而,酶蛋白尤其是多结构域蛋白的活性与稳定性之间的权衡仍然是一个挑战。
该研究拓展了一种计算机辅助策略,通过将非经典氨基酸引入形成硫醚键来“装订”具有多结构域的普鲁兰酶(BtPul)相对柔性的N/C端结构域,以提高其热稳定性。首先利用RosettaMatch算法及自由能预测工具设计并优化溴乙基-酪氨酸在普鲁兰酶N/C末端结构域中的引入位点;其次,采用双质粒共表达的方式在宿主菌中引入目的基因重组质粒的同时引入O2beY正交氨酰-tRNA合成酶/tRNA系统,从而使O2beY能够翻译至目的蛋白中;最终,通过诱导表达实现非天然硫醚键对普鲁兰酶N/C端结构域的“装订”。多个单突变体酶学性质的研究结果显示,最优突变体T73(O2beY)-171C的半衰期较野生型提高157%,Tm值提高7.0 ℃。通过进一步引入亲水性残基增加非天然硫醚键周围疏水表面上的局部亲水性以实现酶的活性-稳定性的平衡,组合突变体T73(O2beY)-171C/T126F/A72R在70 ℃下的半衰期提高211%,酶活增加44%。该研究通过计算机辅助设计非天然共价硫醚键“装订”酶蛋白的方式扩展了酶热稳定改造策略,为其它酶蛋白尤其是多结构域酶的稳定性改造提供了参考。
聂尧教授为论文通讯作者,生物工程学院硕士研究生毕家华为第一作者。上述研究工作得到了国家自然科学基金项目(31872891)、高端外国专家项目(G20190010083)、江苏省六大人才高峰项目(2015-NY-007)、宿迁市酶学重点实验室项目(M201803)、轻工技术与工程一流学科建设项目(LITE2018-09)等的资助。
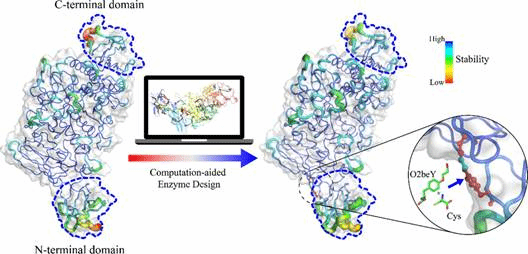
图1 图文摘要
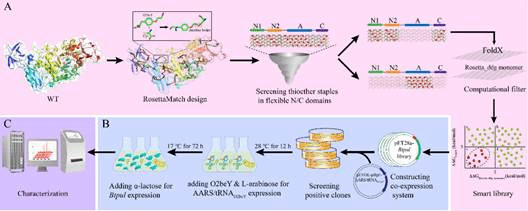
图2 计算机辅助设计的非天然硫醚键提高酶热稳定性流程
