近期,我校生物工程学院和未来食品科学中心陈坚院士团队周景文教授课题组在维生素C一步合成工艺构建方面取得重要进展,研究成果“Efficient production of 2-keto-L-gulonic acid from D-glucose in Gluconobacter oxydans ATCC9937 by mining key enzyme and transporter”正式发表于Bioresource Technology (IF = 11.4) (DOI: 10.1016/j.biortech.2023.129316)。
维生素C是人体必需的维生素之一,也是目前市场销售额最大的维生素。目前所有商业生产维生素C都是通过将2-酮基-L-古龙酸(2-KLG)进行酯化反应之后实现。当前,2-KLG主要生产方式是经典三菌两步法,首先通过高压加氢的方式将葡萄糖转化为山梨醇,然后使用氧化葡萄糖酸杆菌(Gluconobacter oxydans)将山梨醇转化为山梨糖,再通过由普通生酮基古龙酸菌(Ketogulonigenium vulgare)和巨大芽孢杆菌(Bacillus megaterium)组成的混菌发酵体系将山梨糖转化为2-KLG。但随着维生素C的市场需求量逐渐增加,进行产业升级,以更高效和经济的单菌一步发酵模式代替现有生产工艺也显得越发紧迫。直接以葡萄糖为底物通过2,5-DKG途径实现一步发酵合成2-KLG是最有经济价值的替代途径。几十年来,世界范围内的维生素C工业生产领域都在尝试应用更经济的单菌一步发酵路线取代三菌两步发酵过程,但始终没有较大进展。
周景文教授课题组为了开发葡萄糖直接发酵合成2-KLG相关工艺,对该过程中的相关限速环节进行了深入研究和分析。针对葡萄糖合成2-KLG过程中的主要限速问题——如何实现2,5-DKG至2-KLG的高效转化,采用系统优化代谢过程构建高效合成途径的方式实现了2-KLG的高效生成。研究使用G. oxydans ATCC9937作为构建葡萄糖一步发酵合成2-KLG的底盘菌株,发现其天然拥有以葡萄糖为底物直接发酵合成2-KLG的能力,通过基因组分析发现并鉴定内源2,5-DKG还原酶(2,5-DKG至2-KLG转化关键限速酶)。酶学性质分析结果表明该酶催化能力是传统报道中所用的2,5-DKG还原酶的3.15倍(1677 U/mg),更适合用于构建葡萄糖一步发酵合成2-KLG途径。又通过系统代谢分析发现了限制2-KLG产量的其它两个关键因素,分别是底物的转运能力和工程菌株胞内外葡萄糖代谢通量的失衡。通过挖掘具有转运2,5-DKG能力的转运蛋白并在基因组上整合表达,在底盘菌株中实现了转运蛋白的有效表达,解决了底盘菌株底物转运困难的问题。最后,通过发酵过程优化调整了工程菌株胞内外葡萄糖代谢比例,平衡胞内外碳代谢通量,在5 L发酵罐中2-KLG产量达到了30.5 g/L,葡萄糖转化率达到40%。本研究为葡萄糖一步发酵合成2-KLG途径的构建提供了新的可选择的关键限速酶,并对途径中的影响因素进行了全面优化,获得了以葡萄糖一步合成2-KLG报道的最高产量,为实现维生素C一步发酵法的工业化生产提供了重要依据。
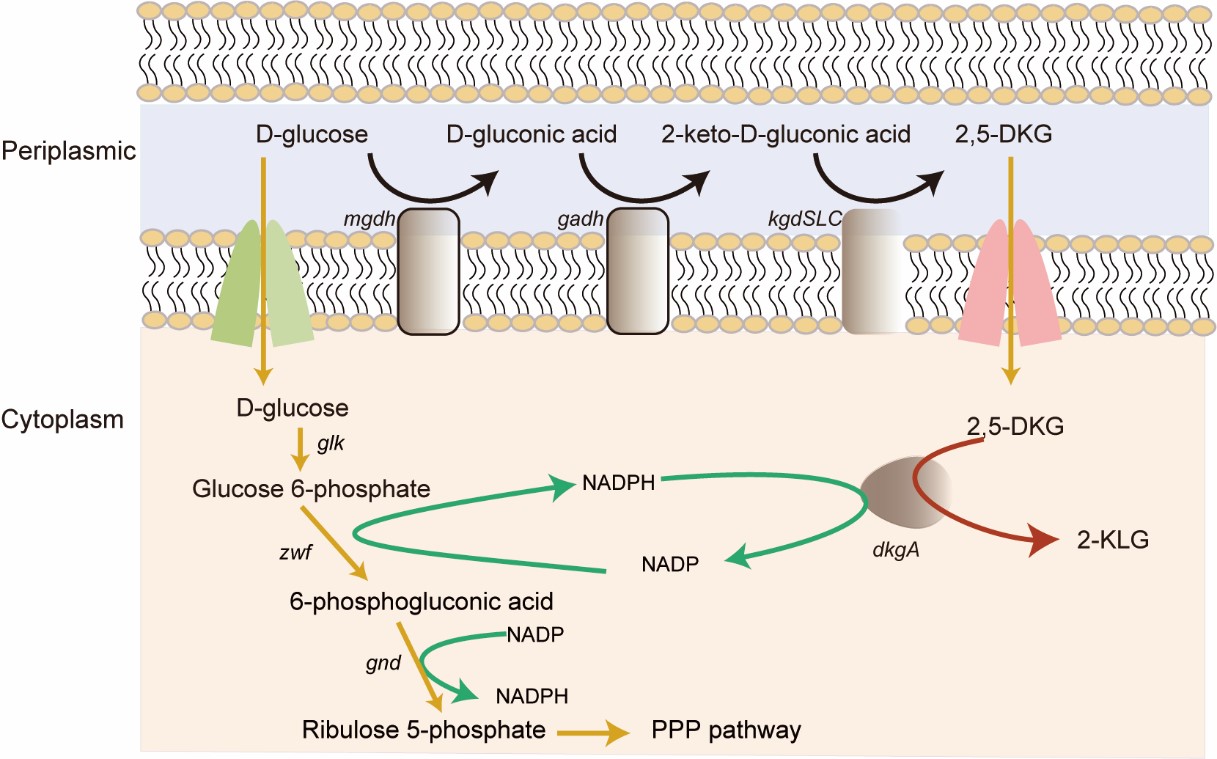
图形摘要
周景文教授为论文的通讯作者,我校2019级博士生李光为第一作者。上述研究得到了国家自然科学基金重点研发项目(31830068)的资助。
近年来,周景文教授课题组以合成生物学科学理论为指导,在系统开展高效合成植物天然产物、维生素、食品功能蛋白等的细胞工厂构建及产业化方面取得丰硕成果,相关研究成果已发表在Nature Communications、Advanced Science、Metabolic Engineering、Bioresource Technology等本领域权威期刊。
